2- MATERIELS ET METHODES
2-1-Sites de prospection
Afin de mener à bien nos recherches, une collection d’échantillons a été faite dans le sud du Bénin, principalement dans les localités de Dangbo ( Tovè ), de Lokossa précisément à Kpinnou, au projet Songhaï de Kinwedji et dans les champs de riz à la station d’Africa Rice.
2-2-Site d’expérimentation
Ce site expérimental se trouve dans le département de l’Atlantique (Sud Bénin), dans la commune d’Abomey-Calavi (6 °C 28 N, 2°C 21 E 15m) à 12 km du Nord Ouest de Cotonou.
2-3-Matériels
2-3-1-Matériels pour tests sérologiques
2-3-1-1-Matériel viral
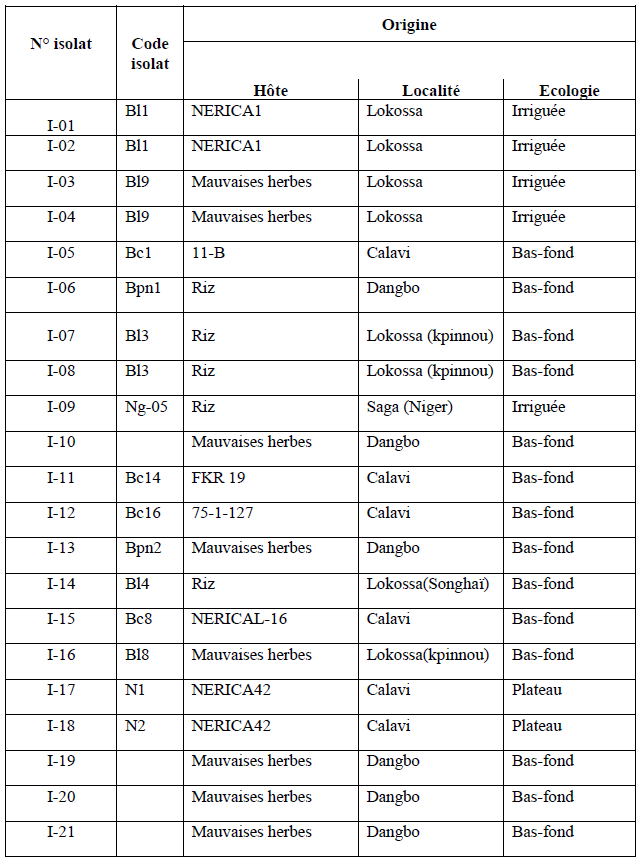
Un total de 21 isolats ont été sélectionnés pour le test sérologique avec l’utilisation d’anticorps polyclonaux et 11 isolats pour le test sérologique avec les anticorps monoclonaux. Nous avons ajouté aux isolats collectés dans le Sud-bénin, un isolat qui nous a été gracieusement offert par Issaka Souley, un étudiant nigérien en thèse.
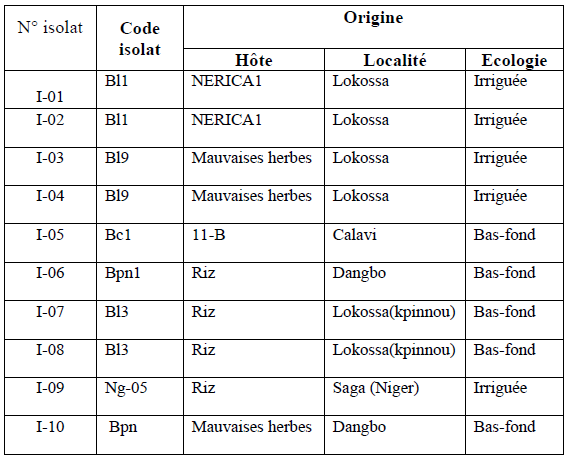
Tableau 1 : Liste des 21 isolats utilisés pour le test sérologique ACP Elisa
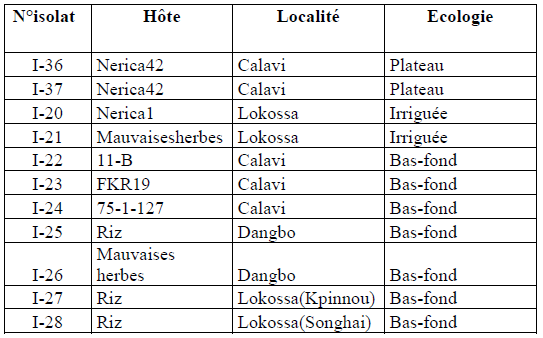
Tableau 2 : Liste des 11 isolats utilisés pour le test Elisa Sandwich Indirect
2-3-1-2-Anticorps utilisés
Les anticorps sont des protéines immunitaires qui réagissent de façon spécifique vis-à-vis du même virus (le même antigène).Ils ont été produit par le laboratoire de phytopathologie d’Africa Rice (Séré et al.,2007 ; Afolabi et al., 2009).
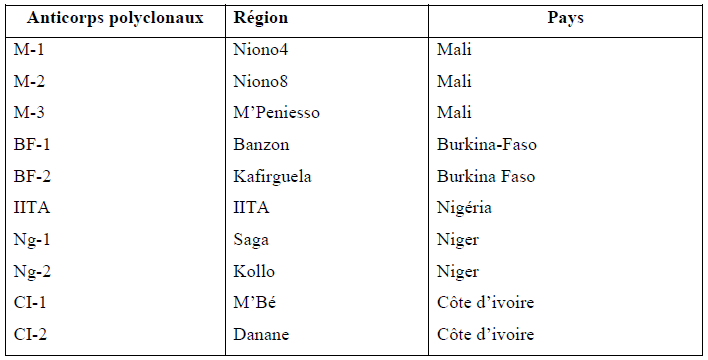
Tableau 3: Liste des 10 anticorps polyclonaux de RYMV utilisés
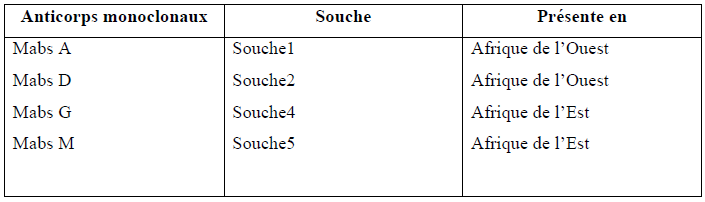
Tableau 4: Liste des anticorps monoclonaux de RYMV utilisés (N’guessan et al.,2000).
2-3-2-Matériels pour test pathogénique
2-3-2-1-Matériel viral
Dix (10) isolats des 21 utilisés pour le test sérologique ont été choisis pour le test pathogénique.
Tableau 5: Liste des 10 isolats utilisés pour le test de pathogénie
2-3-2-2-Matériel végétal
Cinq (05) variétés de riz choisies au sein des variétés établies par l’unité de la phytopathologie du Centre du Riz pour l’Afrique ont été utilisées pour évaluer la pathogénie des différents isolats de RYMV.
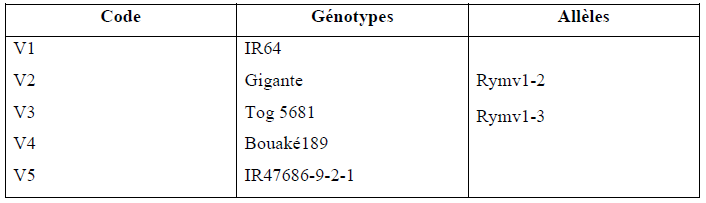
Tableau 6: Liste des 5 variétés utilisées pour le test de pathogénie
2-4- Méthodes
2-4-1-Prélèvement et analyse des échantillons
2-4-1-1 Prélèvement des échantillons
Dans le cadre de cette étude, nous avons débuté par des prospections et collecte des isolats viraux qui ont couvert trois localités du Sud Bénin. La prospection a été effectuée dans les principales zones de riziculture irriguée et de bas-fonds. Les prélèvements ont concerné les espèces de riz cultivées ainsi que des mauvaises herbes.
Les échantillons de feuilles ont été collectés sur la base de l’observation des symptômes attribués à la panachure jaune puis conservées dans une glacière contenant de la glace jusqu’à leur acheminement au laboratoire. Les échantillons ont été ensuite conservés en congélation (-20°C).
2-4-1-2 Détection du RYMV dans les échantillons
La seule présence de symptômes est insuffisante comme outil pour diagnostiquer les maladies fongiques ou virales. Certaines carences notamment celles en fer provoquent des symptômes de jaunissement pouvant être confondus avec les symptômes induits par le RYMV.
Le diagnostic du virus par le test ELISA est un moyen couramment utilisé car elle est généralement fiable et il permet la quantification des virus phytopathogènes.
Le virus de la panachure jaune a été détecté dans les échantillons prélevés au champ par la méthode ACP-ELISA en utilisant un anticorps polyclonal du RYMV (Pabs) selon le protocole décrit en annexe 1.
2-4-1-3 Propagation des isolats
Des extraits d’ échantillons de feuilles collectés au champ ont été utilisés pour propager le virus sur une variété de riz reconnue sensible (IR64) et quatre variétés résistantes : Gigante, (rymv1-2) Tog 5681 (rymv1-3) Tog 5672 (rymv1-4), Tog 5674 (rymv1-5).Ces variétés ont été semées dans des pots en plastique d’une capacité de 5 litres et de 20 cm de diamètre à raison de 3 poquets par pot et de 2 grains par poquet, après pré-germination de ces graines dans des boîtes de pétri. A 21 jours après le semis, les jeunes plants ont été inoculés de façon mécanique à partir des extraits des feuilles obtenus. A cet effet, pour chaque échantillon, les feuilles ont été broyées à l’aide d’un mortier et pilon dans du tampon d’inoculation selon le rapport 1:10 (1 g de feuille dans 10 ml de tampon). Du carborundum a été ajouté au broyat, qui ensuite a été appliqué par friction manuelle aux plantes âgées de 21 jours. L’apparition des symptômes a été suivie et notée respectivement les 28è et 35è jour après l’inoculation (JAI) en utilisant l’échelle de notation des symptômes de l’IRRI (International Rice Research Institute). L’inoculation a été aussi faite sur des variétés résistances pour détecter les isolats les plus virulents (capables de surmonter ces résistances). Ceci a joué un rôle important dans la sélection et le choix des isolats à utiliser pour les différents tests. Pendant toute l’expérience, les pots contenant les plants ont été gardés dans une serre à l’abri des insectes. La température moyenne à l’intérieur de la serre est de 39°C et l’humidité relative de 95.
2-4-2 Tests sérologiques
Suite à la propagation des isolats, 21 isolats ont été sélectionnés pour l’étude du test sérologique. Ces 21 isolats sont soumis au test ACP ELISA, avec l’utilisation de 10 anticorps polyclonaux (Tableau3) mis au point par le laboratoire de phytopathologie de l’ADRAO, (Séré et al., 2007 ; Afolabi et al., 2009). En outre 11 isolats sont soumis au test Elisa Sandwich Indirect avec les anticorps monoclonaux.(Tableau 4) pour connaitre les sérotypes présents au Benin par comparaison à ceux rencontrés dans d’autres pays Africains (N’guessan et al.,2000,).Ce test TAS Elisa a été fait dans le laboratoire de l’IRD – Montpellier en France. (protocole décrit en annexe3).
2-4-3 Test pathogénique
2-4-3-1 Dispositif expérimental
L’essai a été installé suivant le dispositif bloc de Fisher à 3 répétitions, pour chacune des trois techniques d’inoculations testées : la technique d’inoculation par friction manuelle, la technique d’inoculation avec du coton imbibé, et la technique par points de piqûre. Une parcelle témoin, constituée de plants non inoculés est installée par technique.
2-4-3-2 Semis des grains
Des graines préalablement prégermées pendant 72 heures dans des boîtes de pétri ont été repiquées dans des pots en plastique de 20 cm de diamètre, 19 ,5 cm de hauteur et de 5 litres de capacité à raison de 2 graines par poquet et 3poquets par pot. Une semaine après repiquage, un démariage est effectué pour ne laisser subsister qu’un plant par poquet.
2-4-3-3 Inoculation du virus
Chaque isolat est utilisé pour l’inoculation des plantules de 21 jours. Pour cela, la suspension virale est préparée dans du tampon d’inoculation et ajoutée à 0,1% de carborundum ; la même concentration virale est utilisée pour chaque isolat. Etant donné que les techniques d’inoculation ont une influence sur l’expression des symptômes (Sorho, 2006) nous avons chercher à comprendre leur impact sur l’analyse et sur la diversité des isolats du RYMV.
Les trois méthodes d’inoculation sont effectuées pour chaque isolat, sur la dernière feuille dégainée et par 2fois pour s’assurer de bien provoquer la blessure dans la feuille.
– méthode d’inoculation par friction manuelle : le doigt est trempé dans l’inoculum et est frotté sur la dernière feuille dégainée.
– méthode d’inoculation avec du coton : le coton est imbibé dans de l’inoculum et est frotté sur la dernière feuille dégainée.
– méthode d’inoculation avec la séringue : elle se fait par le dépôt d’une goutte d’inoculum avec la séringue par des points de piqûre à la surface de la dernière feuille dégainée.
2-4-3-4 Fertilisation
Une fertilisation minérale sous forme de NPK (10-18-18) et d’urée est appliquée. Le NPK est apporté comme engrais de fond à 21 JAS et l’urée au tallage afin de favoriser le développement des plants et enfin à l’initiation paniculaire.
2-4-3-5 Collecte des données
21 et 42 jours après inoculation, différents paramètres sont mesurés sur les variétés semées.
1-La chlorose visuelle : La notation des symptômes foliaires de la maladie a été faite selon l’échelle de notation standard de L’IRRI. Cette notation s’est faite à 7, 14, 21, et à 42 jours après inoculation. L’incidence de la maladie exprimant la proportion de feuilles attaquées par plant a été évaluée. L’indice de sévérité exprime, l’intensité des dégâts causés sur le plant de riz et évaluer selon la formule proposée par Finisa (2003).
Sévérité=((n1 x 1)+(n3 x 3)+(n5 x 5)+(n7 x 7 )+(n9 x 9)) x 100 /((n1+n3+n5+n7+n9) x 9)
Incidence= (n3+n5+n7+n9)/ (n1+n3+n5+n7+n9)
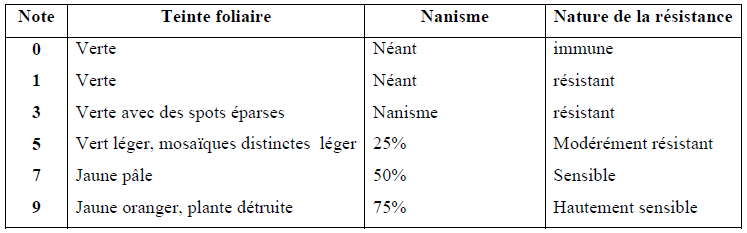
L’échelle de notation comprend 6 classes (Tableau7).
2-La hauteur des plants : Cette mesure se fait à l’aide d’un ruban à 42 jours. Elle se prend de la base du plant jusqu’au niveau du noeud de la panicule la plus haute.
Tableau 7: Echelle de notation de l’évolution de la maladie de la panachure jaune du riz en fonction de l’intensité des symptômes.
Source : IRRI 1998
2-4-3-6-Analyses des données
Le logiciel Excel est utilisé pour recueillir les données et les dépouiller. Les résultats de la sérologie ont été analysés par le système NTSYS-PC version 2.1 (Numerial Taxonomy and multivariate Analyse System) et le dendrogramme est obtenu par UPGMA. L’analyse de variance et la comparaison des moyennes devraient nous permettre de connaitre le degré de différence entre les isolats d’une part et entre les variétés d’autre part. Le modèle statistique AMMI (Additive Main effects and Multiplicative Interaction) utilisé en général pour cerner les interactions Génotype x Environnement devait nous servir à mieux décrire les interactions entre les variétés et les isolats. Cependant en raison d’un manque d’homogénéité des variances rendant impossible l’analyse de variance de la sévérité, nous nous sommes contenter sur le taux de la réduction de hauteur.