1- REVUE DE LA LITTERATURE
1-1- Généralités sur le riz
1-1-1 Origine et taxonomie du riz.
Le riz est une plante annuelle glabre à chaume dressé ou étalé de hauteur variable, allant de moins d’un mètre jusqu’à cinq mètres pour les riz flottants. C’est une plante prédisposée au tallage, formant un bouquet de tiges, à racines fasciculées. Les fleurs, en épillets uniflores, sont groupées en panicules de 20 à 30 cm, dressées ou pendantes. Le fruit est un caryopse enveloppé dans deux glumelles grandes, coriaces et adhérentes, l’ensemble formant le paddy. Selon la texture du caryopse, on distingue les variétés ordinaires, à tégument blanc, le plus souvent, ou rouge ; ou glutineuses (riz gluant, sweet rice). Les variétés de riz africain sont généralement à tégument rouge. Le riz est une céréale de la famille des Poacées ou Graminées ,et cultivée dans les régions tropicales, subtropicales et tempérées chaudes pour son fruit, ou caryopse, riche en amidon. Il désigne l’ensemble des plantes du genre Oryza, parmi lesquelles deux espèces sont cultivées : Oryza sativa et Oryza glaberrima, ou riz de Casamance.
• Oryza glaberrima est née dans la boule du Niger, avant de se propager vers les côtes de Guinée Bissau, Zambie, Sénégal.
• Oryza sativa est d’origine asiatique et se distingue en deux types : Indica et Japonica,
– Indica (originaire de l’Asie Tropicale) riz de bas-fonds, se caractérise par un fort tallage, des feuilles longues et fines, grains longs et fins.
– Japonica (originaire de la zone tempérée et subtropicale de l’Asie) est caractérisé par un tallage moyen, des feuilles assez courtes et fines à grains courts et ronds.
1-1-2 Croissance et développement du riz
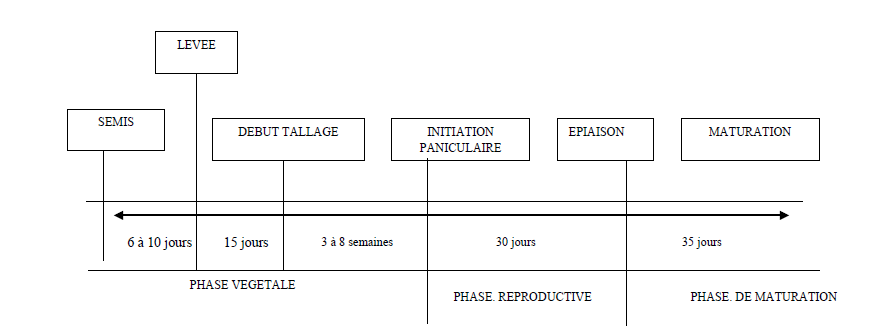
La plante du riz comporte : les organes végétatifs (racines, tiges, et feuilles) et les organes floraux (panicules comportant les épillets). La vie d’un plant de riz se divise en trois phases : La phase végétative qui commence de la germination à l’initiation paniculaire, La phase reproductive qui commence de l’initiation paniculaire à la floraison et La phase de maturation qui commence de la floraison à la maturité
Figure 1 : Croissance et développement du riz
1-1-3 Modes de culture
Le riz est généralement considéré comme une plante de milieu humide et de climat chaud. La culture est réalisée sous différents modes en fonction des régions. Le mode de culture est essentiellement basé sur le niveau d’alimentation hydrique fournie. Ainsi, on distingue trois principaux modes de cultures : culture pluviale, culture irriguée ou riziculture aquatique avec maîtrise totale de l’eau et riziculture de submersion (anonyme, 1991; Jacquot et al., 1997).
En riziculture pluviale, les besoins en eau sont exclusivement fournis par la pluie. Cette eau de pluie peut être captée par une nappe phréatique proche de la surface (riziculture pluviale sur nappe). En absence de nappe phréatique, la riziculture est dite pluviale stricte. Le riz pluvial (upland rice, rainfed) est cultivé en Asie, en Afrique et en Amérique Latine. (FAO, 1997). Le riz pluvial qui dépend de la pluviosité donne des rendements très faibles à cause de l’irrégularité de l’alimentation en eau, de la pauvreté des sols et aussi de la présence fréquente de minéraux toxiques (fer, aluminium, sel) (FAO, 1997).
La riziculture irriguée (irrigated rice) ou de submersion contrôlée est le mode de culture du riz dans lequel il y a maîtrise totale de l’eau aussi bien pour l’irrigation que pour le drainage. La disponibilité et la maîtrise de l’eau permettent ainsi de réaliser deux cycles de culture par an sur une même surface cultivée.
La riziculture de submersion non contrôlée (33% des surfaces cultivées) est exercée dans des zones basses inondées, par les crues ou par l’eau provenant du ruissellement de pluie, pendant une partie du cycle de culture. Un cas particulier de ce type de culture est la riziculture flottante dans laquelle la lame d’eau issue des crues peut atteindre 1 à 5 mètres, les tiges des plants de riz s’allongent en conséquence (CNUCED, 2004).
Au Bénin, trois types de riziculture sont généralement pratiqués : riziculture pluviale stricte, riziculture pluviale de bas-fond, et riziculture irriguée avec une prépondérance pour la riziculture pluviale de bas-fond.
1-2 Ravageurs et maladies du riz
1-2-1 Ravageurs du riz
1-2-1-1 Les insectes
Le riz est l’hôte de plusieurs centaines d’espèces d’insectes, dont une trentaine environ est économiquement importante. Les principaux ravageurs sont les foreurs des tiges, les cicadelles, les mouches à galle (cécidomyie) et les insectes des stocks de grains. Ces insectes induisent des dégâts considérables chaque année, avec des estimations de pertes allant de 0 à 30, parfois 50% du rendement (Arraudeau, 1998). Un très grand nombre de variétés sont mentionnées comme s’étant montrées, une année et dans un lieu donnés, comme résistantes à un ou plusieurs insectes. Les rapports de l’IRRI montrent cependant des changements notables dans les résistances au cours du temps, et la plupart des variétés « IR » données comme résistantes à un insecte donné une certaine année sont citées comme étant devenues sensibles ultérieurement, à de rares exception près. Ceci est une indication claire que la résistance, à laquelle on pense de plus en plus pour juguler les dégâts causés par les insectes, n’est pas stable au cours du temps.
1-2-1-2 Les nématodes
Des travaux portant sur l’inventaire des espèces de nématodes qui parasitent les racines du riz en Asie et en Afrique et sur les dégâts qu’ils provoquent ont été réalisés par IRRI en collaboration avec l’OSRTOM, puis l’IRD entre 1985 et 2000 (Reversat et al., 2003). De ces travaux, il en ressort que deux espèces parasitent les racines selon que l’on est en riziculture irriguée ou en riziculture pluviale. En effet en riziculture irriguée en Asie, comme en Afrique de l’Ouest, le genre Hirschmaniella Luc and Goody, un endoparasite migrateur, prédomine avec plusieurs espèces selon les pays ou les régions. En riziculture pluviale, deux espèces majeures ont été trouvées aux Philippines, en Indonésie et au Vietnam : Meloidogyne graminicola Golden and Bierchfield, un endoparasite sédentaire et Pratylenchus zeae Graham, un endoparasite migrateur. Ce sont également les espèces majeures trouvées en Inde, en Thaïlande mais pas en Afrique (Prot, 1994) .D’une manière générale ces nématodes induisent des symptômes de jaunissement et des dégâts sur les parties aériennes du riz qui ne sont pas spécifiques de l’attaque des racines par les nématodes. Ces symptômes peuvent être confondus, notamment, avec ceux provoqués par une mauvaise nutrition minérale.
1-2-2 Maladies du riz
1-2-2-1 Maladies fongiques
On considère, en général, la pyriculariose (Pyricularia oryzae Cav.Magnaporthe oryzae) comme la principale maladie du riz parce qu’elle est largement répandue (85 pays) et qu’elle peut provoquer des ravages lorsque les conditions sont favorables. Il semble que les microclimats autour des plants de riz pluvial favorisent l’apparition de la pyriculariose. La plantule, le tallage et l’initiation paniculaire sont les stades les plus sensibles aux attaques de la maladie. Des pertes dues à cette maladie allant de 1,4 jusqu’à 100% ont été enregistrées. Le champignon provoque des tâches sur les feuilles, les noeuds et sur différentes parties des panicules et des grains, mais rarement sur la gaine dans la nature. Les tâches ont une forme elliptique avec des extrémités plus ou moins allongées. En général, le centre des tâches est gris ou blanchâtre et le pourtour brun ou brun-rougeâtre. D’autres espèces de champignons sont susceptibles d’attaquer les plantes :échaudure foliaire, gigantisme, la galle blanche.(Sy et Séré,1996).
1-2-1-2 Les nématodes
Des travaux portant sur l’inventaire des espèces de nématodes qui parasitent les racines du riz en Asie et en Afrique et sur les dégâts qu’ils provoquent ont été réalisés par IRRI en collaboration avec l’OSRTOM, puis l’IRD entre 1985 et 2000 (Reversat et al., 2003). De ces travaux, il en ressort que deux espèces parasitent les racines selon que l’on est en riziculture irriguée ou en riziculture pluviale. En effet en riziculture irriguée en Asie, comme en Afrique de l’Ouest, le genre Hirschmaniella Luc and Goody, un endoparasite migrateur, prédomine avec plusieurs espèces selon les pays ou les régions. En riziculture pluviale, deux espèces majeures ont été trouvées aux Philippines, en Indonésie et au Vietnam : Meloidogyne graminicola Golden and Bierchfield, un endoparasite sédentaire et Pratylenchus zeae Graham, un endoparasite migrateur. Ce sont également les espèces majeures trouvées en Inde, en Thaïlande mais pas en Afrique (Prot, 1994) .D’une manière générale ces nématodes induisent des symptômes de jaunissement et des dégâts sur les parties aériennes du riz qui ne sont pas spécifiques de l’attaque des racines par les nématodes. Ces symptômes peuvent être confondus, notamment, avec ceux provoqués par une mauvaise nutrition minérale.
1-2-2-2 Maladies bactériennes : flétrissement bactérien des feuilles
Le flétrissement bactérien des feuilles causé par Xanthomonas oryzae p.v. oryzae Dye] a été décrit surtout en Asie (Japon en Inde, à Sri Lanka, dans les régions du centre-est, du sud et de l’ouest de la Chine, à Taïwan Province de Chine dans la Péninsule coréenne, en Thaïlande au Viet Nam, aux Philippines) dans le nord de l’Australie; dans plusieurs pays d’Amérique latine; à Madagascar; Il a été signalé pour la première fois en Afrique de l’Ouest, au Mali, par Buddenhagen et al .,(1979) ,ensuite au Niger et au Sénégal. Les pertes de rendement, dans les champs gravement contaminés, se situent entre 20 et 30 pour cent et peuvent atteindre 50 pour cent. Les pertes de rendement enregistrées dans certains états de l’Inde varient de 6 à 60 pour cent. Sur les plantules, le flétrissement apparaît tout d’abord comme une petite tâche mouillée à la périphérie des feuilles inférieures pleinement développées. Avec l’extension des tâches, les feuilles jaunissent, sèchent et se fanent. Sur le limbe, les lésions apparaissent en général sur les bords à partir de la pointe et s’agrandissent avec un contour ondulé, puis deviennent jaunes et sèches. Il arrive que les symptômes foliaires soient difficiles à reconnaître. Une méthode simple décrite par Ou (1984) consiste à couper un petit morceau de lésion foliaire et de l’examiner au microscope dans une goutte d’eau, un exsudat bactérien s’écoule des vaisseaux foliaires au bout de quelques minutes.
D’autres maladies bactériennes existent sur le riz en Afrique. En particulier la pourriture bactérienne des gaines causée par Pseudomonas fusco vaginae qui sévit surtout dans les régions froides et en altitude (Ou 1984).
1-2-2-3 Maladies virales
• Le virus tungro du riz :
Le tungro (qui signifie croissance dégénérée) a été observé pour la première fois à l’IRRI, aux Philippines, en 1963. On l’a identifié comme un virus transmis par Nephotettix virescens. Sa présence a été signalée en Malaisie (Penyakit mersh ou maladie rouge), en Indonésie (mentek, midgel), en Thaïlande (feuille jaune-orange) et en Inde (avec un virus ressemblant au tungro), la transmission par N. virescens ayant chaque fois été confirmée. Les principaux symptômes observés sur les plants de riz atteints de tungro sont le rabougrissement et la décoloration des feuilles, dont la teinte varie entre différentes nuances de jaune et l’orange. Le principal vecteur du virus de tungro est N. virescens, bien que le vecteur N. nigropictus ait été signalé par l’IRRI (aux Philippines) et en Thaïlande.
• Rice Hoja Blanca virus (RHBV)
La «Hoja blanca» n’est pas aussi répandue que la pyriculariose en Amérique latine, mais elle est responsable de pertes importantes dans la même zone. «Hoja blanca» est transmise par la delphacide Sogatodes oryzicola (Muir). Des bandes blanches ou chlorotiques apparaissent sur les feuilles de riz, ou bien celles-ci deviennent entièrement blanches. Les plants sont atrophiés et les épillets mal remplis. En Amérique latine, les variétés suivantes ont été identifiées comme résistantes à la «Hoja blanca»: CICA 7. CICA 9, Iniap 415, Iniap 7, Donato et Canilla.
• La panachure jaune du riz
La panachure jaune du riz est une maladie virale inféodée au continent africain et se développe surtout sous écosystème irrigué ou de bas-fond dans différents pays africains dont le Bénin. Cette maladie fera particulièrement l’objet de nos recherches.
1-3 La panachure jaune du riz
1-3-1 Répartition géographique du RYMV
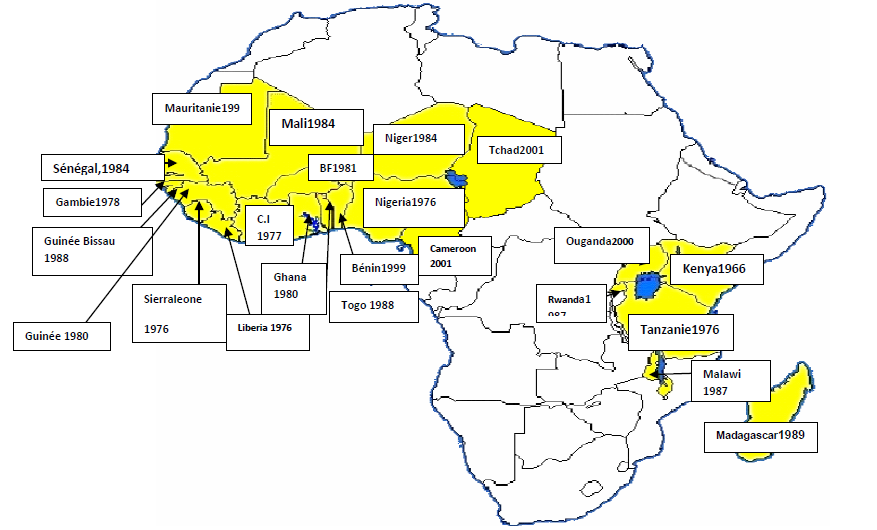
Le virus de la panachure jaune du riz (RYMV) a été d’abord reporté en 1970 dans la province de Nyanza à l’ouest du Kenya près du lac Victoria (Bakker, 1974 ). Par la suite, le virus a été décrit dans de nombreux pays différents de l’Afrique de l’Ouest, Centrale, et orientale. Il a été décrit en 1976 au Libéria, Nigéria, Sierra Leone, et en Tanzanie (Raymundo et Buddenhagen,1976 ; Rossel et al ., ; 1982). Dans la suite des années, le RYMV a été signalé dans plusieurs localités en Côte d’Ivoire (Fauquet et Thouvenel, 1977), et en 1980 au Ghana et Koba en Guinée (Raymundo et Konteh, 1980). À la fin des années 1980, le RYMV avait été identifié au Niger, Burkina Faso, et au Mali, ainsi que dans le Malawi (John et al ., 1984) et Rwanda (Awoderu et al., 1987), et il a été décrit à Madagascar en 1989. Sur cette île, la gravité de l’infection était telle, qu’en quelques années, plus tard, la culture du riz a été abandonnée à Marovoay et au lac Alaotra (Reckhaus et Randrianangaly,1990). Le RYMV a également été aussi reporté en Gambie,(Séré et al.,)Guinée
Bissau, Sénégal, Mauritanie (Awoderu ,1991), et à Zanzibar (Ali et al., 1995). Récemment, le virus a été signalé au Cameroun et au Tchad (Afrique centrale) (Traoré et al., 2001). Le RYMV est limité c’est-à-dire qu’il est endémique à l’Afrique. Il infecte surtout le riz de bas-fond en Afrique de l’Ouest (Rossel, 1986); Toutefois, en 1987, il a également été signalé pour la première fois sur la culture des hautes terres (Awoderu et al., 1987). Lors d’une enquête en 1983 et 1986, 75% des superficies totales cultivées de riz dans le Sahel a été rapporté d’être contaminés, 40% dans la savane du Soudan, 18% en savane guinéenne, et 7,5% dans la forêt tropicale humide (Awoderu, 1991). L’incidence et la sévérité de la maladie semblent dépendre selon les variétés de riz, l’environnement, et des zones de végétation (Awoderu, 1991).
1-3-2 Importance économique du RYMV
L’impact économique du RYMV est difficile à évaluer en raison de l’influence de nombreux facteurs tels que l’environnement d’une zone de végétation, et les variétés de riz. Les pertes de rendement fluctuent entre 10 et 100% selon l’âge des plantes avant l’infection, la sensibilité de la variété de riz, de l’environnement et des facteurs climatiques. Une enquête de l’Office du ” Niger” au Mali a montré des pertes de récolte jusqu’à 70% des infections au RYMV.
Les réductions de rendement variant de 58 à 68% ont été signalées en 1986 dans la République du Niger (Reckhaus et Adamou, 1986). Une autre étude réalisée par Taylor (1989) indique des pertes de rendement de 82 à 97% sur les variétés PN623-3, Tox 516-12-SLR, ROK3, ROK15, et IR65.
Figure 2 : Répartition géographique du RYMV
1-3-3 Structure, cycle du RYMV
• Structure du virus
Les caractéristiques structurales et biochimiques du RYMV ont permis de le classer dans le groupe des sobémovirus. Les virus du groupe des sobémovirus sont caractérisés par des particules virales isométriques de 25 à 28 nm de diamètre, sans enveloppe et composés de 180 molécules d’une seule protéine capsidiaire (PC) de masse moléculaire estimée à 30kD. Leur structure tridimensionnelle a été déterminée par cristallographie aux rayons X à une résolution de 2,8 Å (Qu et al., 2000; Opalka et al., 2000). La capside virale présente une symétrie icosahédrale de type T=3. Elle est constituée de 180 sous unités de la protéine de capside. Chaque sous-unité protéique est composée de deux domaines, l’un interne dit domaine R (random) et l’autre appelé domaine S (surface ou Shell). Le domaine R serait impliqué dans les interactions entre l’ARN viral et les sous-unités protéiques ainsi que dans les repliements de l’ARN lors de l’assemblage des virions (Hull, 1988). Le génome du RYMV est composé d’une molécule d’acide ribonucléique simple brin de masse moléculaire 1,4×106 DA (Bakker, 1974). L’ARN non polyadenylée, de polarité positive est liée de façon covalente par son extrémité 5’ à une protéine (Vpg) et composée de 4450 nucléotides constitués en quatre cadres ouverts de lecture. Le génome est compact et la plupart des ORF se chevauchent. L’ORF1 code pour une protéine dite P1 qui intervient dans le mouvement du virus dans la plante (Bonneau et al., 1998). L’ORF2 donne par traduction une polyprotéine qui est clivée par la suite pour donner deux protéines fonctionnelles (une protéase à sérine et la VPg) et un ARN polymérase ARN-dépendante (RdRp). L’ORF4 code pour la protéine de capside par l’intermédiaire d’un ARN sub-génomique de 1010 nucléotides. Cependant Le rôle de l’ORF3 n’a pas été élucidé. Un ARN satellite est souvent associé au RYMV. L’ensemble du génome comporte trois régions non codantes. La première région sépare les ORF 1 et 2 et la troisième située à l’extrémité 3’ contient un domaine de pseudo noeuds permettant la stabilisation de l’ARN génomique entier.
• cycle viral
Dans le cycle, on distingue différentes étapes, qui se chevauchent :
1-Pénétration dans la cellule : décapsidation
2-Traduction : le message viral est traduit par les ribosomes cellulaires qui synthétisent les protéines virales. Ces protéines interviennent dans une ou plusieurs fonctions comme la réplication, le mouvement, la transmission, la protection etc.
3-Réplication : copie par complémentarité de l’acide nucléique du virus pour donner de nombreux exemplaires
4-Encapsidation : acides nucléiques et protéines s’assemblent spontanément pour former de nouvelles particules virales.
Toute propriété de la plante susceptible d’interférer l’une des étapes du cycle, peut être considérée comme un facteur de résistance à la maladie (Mansky et Hill, 1993).
1-3-4 Symptômes de la maladie
Les symptômes de la panachure jaune du riz ont quatre caractéristiques principales sur un plant de riz et ce sont elles qui montrent comment s’effectue la perte de rendement. En effet, elle se manifeste par un jaunissement et/ou une coloration orange des feuilles (la chlorose), des nécroses, une réduction du tallage, un rabougrissement des plants, la réduction de l’exsertion paniculaire et la stérilité des panicules (WARDA, 2000; Sarra, 2005).Les premiers symptômes de la maladie sont des points chlorotiques se développant sous forme de stries. Les tâches jaunes évoluent généralement vers une décoloration totale des feuilles qui deviennent jaune-oranger (Raymundo et Buddenhagen, 1976 ; Fauquet et Thouvenel, 1977).
La chlorose est la réduction de la pigmentation verte. Comme la pigmentation verte des feuilles constitue l’indispensable chlorophylle qui capte l’énergie, la chlorose réduit la photosynthèse et par conséquent une croissance de la plante. Le rabougrissement se réfère à une réduction sévère de la taille de la plante : les plants de riz infectés sont beaucoup plus courts que les plants sains. Les panicules portent les grains de la plante et sont donc essentielles à un bon rendement. Dans les champs infestés de panachure jaune du riz, les panicules ne poussent pas normalement (WARDA, 2000). En outre, beaucoup de grains des panicules infestées sont stériles (Kouassi et al., 2005). Lorsque l’infection est précoce (avant deux semaines après le semis), les plantules des cultivars sensibles meurent. L’infection de la parcelle peut se présenter sous diverses formes. En effet des parcelles avec un taux d’infection élevé ou complètement infectées peuvent être contiguës à des parcelles sans infection apparente (Sarra, 2005). De larges ou petites tâches en formes irrégulières ou cicatricielles apparaissent dans certaines rizières alors que ce sont de petites tâches allongées qui sont occasionnellement observées le long des digues, des pistes et aux angles de la parcelle. Ces différentes formes de symptômes sur les parcelles indiquent une propagation de la maladie par plusieurs mécanismes (bétail, eau d’irrigation, outils aratoires) (Sarra, 2005). Les rizières infectées présentent en général un aspect jaune orange.
Figure 3 : Symptômes caractéristiques du RYMV
1-3-5- Mode de transmission et épidémiologie
Les deux types de transmission du RYMV qui sont clairement admis sont les suivants: la transmission par les insectes et la transmission par inoculation artificielle mécanique. Bakker (1974) signale en Afrique de l’Ouest plusieurs espèces de coléoptères qui ont le potentiel de transmettre le virus, aux plantes notamment les Sesselia pussilla Gerstaecker(Galerucinae), Chaetocnema pulla Chapius (Halticinea), Chaetocnema dicladispa (Chrysispa) Kraatz (Hispinae), et Trichispa sericea Guerin (Hispinae). Cependant, le rôle de ces vecteurs dans les épidémies du RYMV. n’est pas bien établi. En Afrique orientale, Bakker (1974) rapporte que des plants de riz malades ont été systématiquement trouvés aux frontières des parcelles de riz le long des diguettes d’irrigation, ce qui suggère la transmission du virus par des insectes vecteurs à partir de sources externes. A l’office du Niger, au Mali, Peters (1996) a trouvé des exploitations rizicoles complètement infectées du RYMV à côté des exploitations indemnes de virus, ce qui suggère que les vecteurs jouent un rôle mineur dans la propagation du virus. Il a été formellement établi que l’infection au RYMV n’est pas transmis par les semences (Bakker 1974; Fauquet et Thouvenel 1977; Konaté et al., 2001) même si le virus a été détecté dans toutes les pièces de semences de riz (lemme, caryopse, et embryon) (Abo 1998; Konaté et al., 2001). Konaté et al., (2001) ont montré que l’absence de transmission est due à l’inactivation du virus pendant la phase de maturation de la graine de riz.
La transmission abiotique du RYMV a été fortement soupçonnée mais n’a pas encore été démontrée. Selon Reckhaus et Andriamasintseheno (1995), le repiquage du riz dans un sol contenant de la bouse de vache et mal décomposée, et des résidus de culture infectés pourraient être responsables de la transmission mécanique du RYMV. Les mêmes types de transmission ont pu être observés quand le riz est transplanté dans un sol sur lequel les repousses de riz touchées, et les racines ont été manipulées lors des opérations de labour (Abo, 1998). Le RYMV aurait pu être aussi transmis mécaniquement par le contact du liquide de la guttation et de l’eau d’irrigation avec les plants de riz (Bakker, 1974). Le rôle des hommes dans la transmission mécanique du RYMV est fortement suspecté, surtout pendant des opérations culturales telles que le repiquage, l’application d’engrais, irrigation, récolte. D’autres hypothèses émises ont révélé une probable transmission entre le contact outils agricoles infectés et des plants de riz, entre des mains contaminées et plants de riz, et entre les plantes saines et malades sous l’effet du vent, des hommes, ou animaux (Abo, 1998). L’infection des exploitations rizicoles dans les pépinières infectées par contact entre les plants malades et sains, ou entre des mains contaminées et des plants de riz a été suspectée dès 1974 par Bakker, mais il n’était pas en mesure de le démontrer. L’observation a prouvé que l’infection au RYMV est toujours plus sévère dans les exploitations agricoles avec du riz transplanté que dans des exploitations à l’ensemencement direct et une telle hypothèse a été confirmé par Sy (1994).
1-3-6 Gammes d’hôtes
Les hôtes du virus sont limités à la famille des graminées et Eragrostidae. Plusieurs hôtes artificiels du RYMV ont été identifiés (Bakker, 1974). En Afrique Centrale, Traoré et al.,(2001) ont rapporté une infection naturelle d’Oryza barthii, O.longistaminata, Panicum subalbidum Kunth, Acroceras zizanioides, Sacciolepis africana, Eragrostis sp, Setaria longistaminata, Panicum subalbidum Kunth, Acroceras zizanioides, au Cameroun et au Tchad. En Afrique de l’Ouest, Konaté et al. (1997) ont montré que Echinochloa colona L. Link, Ischaemum rugosum, Salib Panicum repens L., Oryza longistaminata A. Chev. Et Roehr., O. barthii A. Chev étaient infectés naturellement par le RYMV. Le genre Oryza a été rapporté comme le principal hôte naturel du RYMV. Jusqu’en 1996, Oryza longistaminata A. Chev. et Roerh était reconnue comme le seul hôte naturel sauvage du RYMV.
1-3-7 Variabilité sérologique, moléculaire et pathogénique du RYMV
1-3-7-1 Variabilité sérologique et moléculaire
Le RYMV est un virus très variable (Mansour et Baillis, 1994). Sa variabilité sérologique a été mise en évidence à l’aide d’anticorps polyclonaux et monoclonaux discriminants, puis par séquençage partiel ou complet d’isolats de référence originaires de l’Afrique de l’Ouest et de l’Afrique de l’Est y compris le Madagascar. En effet six souches majeures de RYMV ont été décrites dont trois (S1, S2, S3) en Afrique de l’Ouest se trouvant dans les zones de forêts et de savanes, et les trois autres (S4, S5, S6) en Afrique de l’Est (Traoré et al., 2005). En Côte d’Ivoire les souches S1 et S2 sont présentes, S2 étant prédominantes en zones de forêts et S1 en zones de savanes (N’Guessan et al., 2000; 2001). Après analyse, il ressort de ces études que le virus est né en Afrique de l’est et s’est ensuite diffusé à l’ouest et au centre du continent, entraînant une perte subséquente de la diversité génétique (Abubakar et al., 2003). Cette distribution géographique des souches a mis en évidence une relation possible entre variation sérologique et origine écologique des isolats (Traoré, 2006). Cependant, aucune relation de ce type n’avait pu être mise en évidence par Mansour et Baillis (1994) probablement à cause de l’utilisation d’anticorps polyclonaux pour caractériser les variantes sérologiques (Traoré, 2006), et en raison d’un faible nombre d’échantillons et d’anticorps utilisés.
En effet, étudiant à l’aide de 26 anticorps polyclonaux, la diversité sérologique de 42 isolats collectés dans 5 pays d’Afrique de l’ouest, Séré et al., (2005) ont pu mettre en évidence une diversité à l’échelle d’un même champ. Cinq sérotypes parmi les six ont pu être assignés à cinq souches moléculaires suite au séquençage du gène de la protéine de la capside et à l’analyse des séquences obtenues (Pinel et al., 2000; Fargette et al., 2002). Cette concordance entre typages moléculaires et sérologiques constitue donc un atout majeur dans l’étude de la variabilité sérologique du RYMV.
1-3-7-2 Variabilité pathogénique
Contrairement à la variabilité sérologique et moléculaire, peu d’études ont été consacrées à la variabilité pathogénique du RYMV et de plus les informations actuellement disponibles sur la pathogénie sont fragmentaires (Traoré, 2006). La pathogénie est le processus par lequel un parasite agit sur un organisme pour induire une maladie. On peut décomposer le pouvoir pathogène des virus en virulence et en agressivité (Van Der Plank 1968). La virulence est la capacité d’une souche à infecter une variété possédant une résistance à ce virus. Une souche est virulente si elle est capable de se multiplier ou de provoquer une maladie chez une variété possédant une résistance. L’agressivité exprime l’intensité des symptômes chez une variété dans laquelle l’infection peut se développer. Par exemple, une souche sera plus ou moins agressive selon qu’elle induira des symptômes de mosaïque plus ou moins forts (Astier et al., 2001). Les critères pour évaluer l’agressivité d’un virus sont en conséquence : le taux d’accumulation virale, les symptômes foliaires et l’impact sur la production et sur la croissance.
Une étude (Onasanya et al., 2006) sur la pathogénie du RYMV est fondée sur les données de huit (08) variétés différentielles inoculées avec dix (10) isolats différents provenant du Mali. Les variétés ont été classées selon les symptômes et l’impact sur la production. Grâce à cette étude, il a été mis en évidence une relation significative entre l’intensité de la maladie et l’ensemble composé subséquente de la diversité génétique (Abubakar et al., 2003). Cette distribution géographique des souches a mis en évidence une relation possible entre variation sérologique et origine écologique des isolats (Traoré, 2006). Cependant, aucune relation de ce type n’avait pu être mise en évidence par Mansour et Baillis (1994) probablement à cause de l’utilisation d’anticorps polyclonaux pour caractériser les variantes sérologiques (Traoré, 2006), et en raison d’un faible nombre d’échantillons et d’anticorps utilisés. En effet, étudiant à l’aide de 26 anticorps polyclonaux, la diversité sérologique de 42 isolats collectés dans 5 pays d’Afrique de l’ouest, Séré et al., (2005) ont pu mettre en évidence une diversité à l’échelle d’un même champ. Cinq sérotypes parmi les six ont pu être assignés à cinq souches moléculaires suite au séquençage du gène de la protéine de la capside et à l’analyse des séquences obtenues (Pinel et al., 2000; Fargette et al., 2002). Cette concordance entre typages moléculaires et sérologiques constitue donc un atout majeur dans l’étude de la variabilité sérologique du RYMV.
1-3-7-2 Variabilité pathogénique
Contrairement à la variabilité sérologique et moléculaire, peu d’études ont été consacrées à la variabilité pathogénique du RYMV et de plus les informations actuellement disponibles sur la pathogénie sont fragmentaires (Traoré, 2006). La pathogénie est le processus par lequel un parasite agit sur un organisme pour induire une maladie. On peut décomposer le pouvoir pathogène des virus en virulence et en agressivité (Van Der Plank 1968). La virulence est la capacité d’une souche à infecter une variété possédant une résistance à ce virus. Une souche est virulente si elle est capable de se multiplier ou de provoquer une maladie chez une variété possédant une résistance. L’agressivité exprime l’intensité des symptômes chez une variété dans laquelle l’infection peut se développer. Par exemple, une souche sera plus ou moins agressive selon qu’elle induira des symptômes de mosaïque plus ou moins forts (Astier et al., 2001). Les critères pour évaluer l’agressivité d’un virus sont en conséquence : le taux d’accumulation virale, les symptômes foliaires et l’impact sur la production et sur la croissance.
Une étude (Onasanya et al., 2006) sur la pathogénie du RYMV est fondée sur les données de huit (08) variétés différentielles inoculées avec dix (10) isolats différents provenant du Mali. Les variétés ont été classées selon les symptômes et l’impact sur la production. Grâce à cette étude, il a été mis en évidence une relation significative entre l’intensité de la maladie et l’ensemble composé par les pertes de production, la reproductibilité des interactions isolats/variétés et l’existence de trois (3) catégories d’interactions variétés-isolats. De même, les résultats sur les études (Traoré et al., 2006) de la pathogénie de 270 isolats de RYMV collectés dans cinq pays de l’Afrique, dont trois pays de l’Afrique de l’Ouest (Burkina Faso, Mali et Togo) et deux du Centre (Cameroun et Tchad) en zones de savanes soudano-sahéliennes suite à des inoculations à une variété sensible (BG 90-2) et à deux variétés résistantes (Tog5681 et Giganté). Les résultats ont montré que tous les isolats ont induit des symptômes chez BG 90-2 et qu’environ 37% des isolats ont été capables d’infecter les variétés résistantes TOG5681 et Giganté. Ces deux variétés de riz ont présenté des réactions différentes. En effet, une partie des isolats ont pu contourner la résistance chez Giganté seule, une deuxième partie l’a fait chez TOG5681 seule tandis qu’une dernière partie a contourné la résistance chez les deux variétés à la fois. Ces isolats contournant la résistance ont été identifiés dans tous les pays de collecte avec toutefois des fréquences variables : Mali (12%), Burkina (54%), Togo (4%), Cameroun (9%) et Tchad (21%). Enfin des études sur la pathogénie conduites sur un ensemble de lignées et de variétés de référence à l’ADRAO ont fait apparaître d’importantes différences d’agressivité entre les isolats, mais pas de corrélation stricte avec la classification moléculaire des souches de RYMV. Quelques interactions spécifiques entre isolats et variétés ont été observées, et des variétés étroitement apparentées ont présenté des réactions très différentes à l’inoculation, ce qui confirme la complexité de la pathogénie du RYMV (N’Guessan et al., 2001, Hadonou ,2006).
1-3-8 Moyens de lutte
1-3-8-1 Lutte agronomique
Le contrôle cultural a été défini comme la manipulation de l’agro-écosystème afin de le rendre défavorable aux insectes vecteurs ou nuisibles et d’améliorer les conditions de culture des plantes et de développement des ennemis naturels de ces insectes nuisibles (Nwilene, 1999). Ainsi, pour lutter contre le RYMV, plusieurs recommandations ont été faites aux paysans à Madagascar, au Mali, au Niger et en Côte d’ivoire à trois niveaux. Ce sont: (1) le choix des variétés (2) l’infection de la pépinière et (3) propagation de l’infection dans la pépinière.
– Choix des variétés
Les risques d’épidémies peuvent être réduits par: (i) La diversification des variétés bien orientée sur des cultivars tolérants; (ii) La substitution des cultivars sensibles, tel que la BG 90-2 par des cultivars plus tolérants, (iii) La diversification des variétés cultivées dans la même parcelle.
– Lutte contre l’infection de la pépinière
Pour éviter l’infection à ce niveau : (i) Toujours installer les pépinières dans les parties non contaminées de la rizière; (ii) Maintenir propres les digues, les drains et les canaux d’irrigation autour de la pépinière;(iii) Utiliser du fumier non contaminé et bien décomposé; (iv) Interdire l’accès des pépinières aux animaux. (v) Une alternance des sites de pépinière.
– Lutte contre la propagation de l’infection dans la pépinière
La propagation de la maladie peut être évitée par: (i) Elimination immédiate et avec précaution du ou des plantules présentant des symptômes de la maladie, (ii) Le désherbage chimique de la pépinière si nécessaire en utilisant un herbicide tel que le Loudax DF 60 à la dose de 100g/ha, (iii)éviter les déplacements dans la pépinière ,(iv), La Protection de la pépinière contre les rats et les animaux tels que les boeufs et les ânes (Sarra et Peters,2003), (v)La suppression de l’irrigation en contre saison pour se prémunir d’un accroissement de la population des insectes (WARDA, 2000 ; Sarra, 2005).
1-3-8-2 Lutte génétique
– Les résistances naturelles
Comme pour beaucoup d’autres virus, l’utilisation des variétés résistantes semble être le moyen le plus prometteur pour lutter contre le RYMV, (Albar et al., 2006). Des sources de résistance au RYMV ont été mises en évidence chez les espèces de riz cultivées. Une résistance élevée de type monogénique a été identifiée chez la variété Giganté de l’espèce O. sativa indica et chez quelques variétés de l’espèce O. glaberrima (notamment Tog 5681) (Thottapilly et Rossel, 1993; Ndjiondjop, 1999; Albar et al., 2003). Cette résistance élevée se manifeste par une absence de symptômes lors de l’infection et une faible teneur en virus (Ndjiondjop, 1999; Ioannidou et al., 2000). Des études de cartographie ont montré que la résistance au RYMV dans la variété Giganté est basée sur un gène récessif unique se trouvant sur le chromosome 4. Par ailleurs une résistance partielle de type polygénique a été caractérisée chez la variété Azucena de l’espèce O. sativa japonica (Albar et al., 1998). Elle se caractérise par un retard dans l’apparition des symptômes et dans l’accumulation virale (Ioannidou et al., 2000, Ndjiondjop, 2001). Par ailleurs d’autres résistances sont aussi déterminées par un gène récessif rymv1 (4allèles): rymv 1-1 : sensible, rymv1-2 : Giganté, rymv1-3 :Tog5681, rymv1-4 :Tog5672, rymv1-5 :AC96.
Des études ultérieures se sont fondées également sur la cartographie pour identifier des loci à effets quantitatifs (QTL) et des marqueurs génétiques de résistance. Pour cela, une population de lignées haploïdes doublées IR64 x Azucena a été utilisée et les résultats ont montré que la résistance au RYMV était sous un contrôle polygénique accompagné d’interactions complexes entre les QTL, le patrimoine génétique et la morphologie de la plante (Albar et al., 1998): Quinze QTL ont donc été découverts sur sept segments chromosomiques. Ces études ont également permis de détecter un QTL majoritaire localisé sur le chromosome 12 d’une lignée quasi iso-génique (NIL) résistante d’IR64 qui est associé au ralentissement du mouvement des virus dans la plante, notamment au niveau du passage des gaines péri vasculaires-phloème. (Ioannidou et al., 2000). Ces sources de résistance ont été introduites par croisement dans des variétés sensibles à fort potentiel de rendement. Plusieurs descendants de ces croisements sont en cours d’évaluation. Parmi eux les variétés du groupe NERICA (New Rice for Africa, issu du croisement entre riz africain Oryza glaberrima et riz asiatique Oryza sativa) sont présentées comme prometteuses du fait qu’elles présentent d’autres atouts comme la résistance aux mauvaises herbes, aux ravageurs et aux maladies, au déficit hydrique, etc. De même pour créer des variétés populaires à haut rendement résistantes au RYMV, le gène de résistance (se trouvant sur le chromosome 4) a été transféré dans trois variétés Oryza sativa largement cultivées. Des hybrides F1 et des plants BC1F1 ont été développés et la sélection par marqueurs a permis la sélection des plants BC1F1 résistants pour le développement des descendances BC2F1 (ADRAO, 2003).Plus récemment un gène de résistance majeure baptisé Rymv1 a été identifié par Laurence Albar et al. (2006) à l’IRD Institut de Recherche pour le Développement. Ce gène serait lié à une fonction biologique essentielle de la plante puisqu’il permet de traduire les ARN messagers cellulaires en protéines. Les chercheurs ont également montré que chez quelques variétés, de petites mutations dans une zone particulière de ce gène seraient responsables de la production des allèles de résistance différents dans le cultivar Giganté et dans les variétés résistantes Tog5681 et Tog5672. Selon des hypothèses préalables, chez une variété sensible à l’infection, le virus interagit avec le facteur codé par le gène et l’utilise à son propre avantage. Ces recherches permettront à terme de faciliter le transfert de ce gène par croisements entre variétés résistantes et variétés sensibles mais à fort potentiel de rendement (Albar, 2006).
– Le contournement de la résistance élevée
Dans le cas particulier du RYMV, des programmes de criblage ou de création variétale ont été ou sont en cours. Au cours de ces dernières années, des sources de résistance naturelle caractérisées ont été introgressées par croisement dans des variétés d’intérêt économique. La résistance élevée s’est avérée la plus efficace. Le déploiement de ces variétés dans les champs est envisagé à brève échéance. Les perspectives offertes par ces variétés seront directement fonction de la durabilité de leur résistance. Malheureusement on a constaté que ces résistances peuvent être contournées soit par des isolats virulents existant dans les champs (Konaté et al., 1997; Sorho et al., 2005; Traoré, 2006), soit émergent après des séries d’inoculation (Fargette et al., 2002; Traoré et al., 2006). Ainsi il a été montré que plusieurs cycles d’inoculations en série effectuées sur les variétés hautement résistantes Tog5681 et Giganté pouvaient entraîner l’émergence des isolats capables de contourner la résistance (isolats dits RB pour Resistance Breaking). Les travaux de Traoré et al., (2006) ont montré que sur 280 isolats collectés dans cinq pays de l’Afrique, 38.6% des isolats étaient capables d’infecter les deux variétés résistantes Tog5681 et Giganté. Ces isolats RB ont été identifiés dans tous les pays avec toutefois des fréquences variables. La grande distribution ainsi que la fréquence élevée de ce type d’isolats pourraient être une sérieuse menace pour la durabilité des résistances mises au point contre le RYMV. Selon Sorho et al., (2005) le risque de contournement est d’autant plus élevé que la pression d’inoculum est plus forte. Une mutation dans le Virus-Protein Genome linked (Vpg) du RYMV serait responsable du contournement (Hébrard et al., 2006).
La panachure jaune du riz a été découverte au Bénin en 1999 .Depuis, très peu de travaux ont été consacrés aux isolats du virus de ce pays. L’importance économique de la maladie, son épidémiologie et la variabilité sérologique de son agent pathogène y restent méconnues. A l’heure actuelle, seule la souche S1 a été découverte au Bénin (Sorho,2006).
Une synthèse bibliographique sur le riz et les maladies virales, notamment la panachure jaune du riz aide à préciser les objectifs de ce travail . Puis, les matériels et les méthodes utilisés sont décrits avant de donner les résultats obtenus. Enfin, les résultats et leurs implications sont discutés afin de tirer les conclusions et perspectives qui s’imposent.